De 5 a 9 de novembro, horário local, a 58ª Semana do Rim 2025 da Sociedade Americana de Nefrologia (ASN) foi realizada em Houston, Texas. Como principal evento acadêmico global no campo da nefrologia, esta conferência revelou vários avanços significativos na pesquisa no tratamento da nefropatia por IgA (IgAN). Este artigo fornece uma visão geral dos-desenvolvimentos e tendências de ponta no tratamento de IgAN sob diversas perspectivas, incluindo medicamentos de pequenos ácidos nucleicos, terapias com anticorpos e medicamentos de moléculas pequenas.
01 Pequenos Medicamentos de Ácido Nucleico
No espaço de pequenos medicamentos de ácidos nucleicos, as empresas farmacêuticas inovadoras nacionais demonstraram fortes capacidades de I&D.
Na conferência deste ano, a Frontage Biotech apresentou dados abrangentes de eficácia pré-clínica para dois de seus medicamentos de pequenos ácidos nucleicos desenvolvidos de forma independente: o FB7013 de alvo único-, que tem como alvo MASP-2, em um modelo de IgAN em macaco cynomolgus, e os dados de eficácia pré-clínica mais recentes para o FB7011 de alvo duplo no mesmo modelo.
FB7013: O primeiro medicamento siRNA direcionado ao MASP-2
O FB7013 é atualmente o primeiro medicamento de siRNA direcionado ao MASP-2, um fator-chave na via da lectina, e é promissor como uma nova opção terapêutica baseada em mecanismo-para IgAN e outras doenças mediadas-pelo complemento. Os dados apresentados na conferência mostraram que o FB7013 alcançou mais de 90% de supressão do mRNA de MASP2 in vitro, com uma concentração inibitória metade da máxima (IC50) na faixa picomolar. Num modelo de ratinho transgénico MASP2 humanizado, uma dose única resultou no silenciamento sustentado do ARNm de MASP2 do fígado durante até dois meses. Em macacos cynomolgus, o FB7013 alcançou a supressão da expressão da proteína MASP2 por até quatro meses, com efeitos estatisticamente significativos.
Estes resultados indicam que o FB7013 proporciona uma inibição potente e durável da ativação da via da lectina. Do ponto de vista farmacodinâmico, o medicamento pode apoiar um regime de dosagem de uma vez a cada seis meses em humanos, potencialmente abordando os desafios atuais relacionados à eficácia e à frequência de dosagem.
FB7011: Sinergia de-alvo duplo para "Interceptação-de caminho duplo"
O FB7011 tem como alvo inovador tanto a via da lectina (MASP-2) quanto a via alternativa (CFB), um projeto de "interceptação de via dupla" não relatado anteriormente em pequenas moléculas existentes ou medicamentos com anticorpos monoclonais. Dado que a ativação do complemento na IgAN envolve frequentemente tanto a lectina como as vias alternativas, o FB7011 demonstra vantagens mecanísticas únicas.
Dados pré-clínicos mostraram que o FB7011 inibiu o mRNA de MASP2 e CFB em mais de 90% in vitro, com valores de IC50 na faixa picomolar. Em modelos de camundongos transgênicos duplos e de macacos cynomolgus, uma dose única silenciou efetivamente o mRNA de CFB e MASP2, ao mesmo tempo que inibiu a expressão da proteína MASP2. Não foram observados efeitos fora do alvo ou imunotoxicidade in vitro, e o FB7011 exibiu boa tolerabilidade in vivo. Seu perfil farmacodinâmico pode suportar um regime de dosagem semestral-em humanos.
Tanto o FB7011 quanto o FB7013 são pequenos medicamentos de ácido nucleico direcionados ao sistema complemento, apresentando mecanismos de ação inovadores. Eles têm o potencial de aumentar significativamente a eficácia e a segurança do tratamento com IgAN e melhorar a adesão à medicação do paciente. Além da IgAN, esses dois medicamentos também poderiam ser expandidos para tratar outras doenças causadas pela ativação anormal do complemento em longo prazo - incluindo nefropatia membranosa primária (PMN),-degeneração macular relacionada à idade/atrofia geográfica (DMRI/GA) e doença renal diabética (DKD) - oferecendo novas opções terapêuticas para uma população mais ampla de pacientes.
SGB-9768 da Sylentis: uma terapia de RNAi visando C3
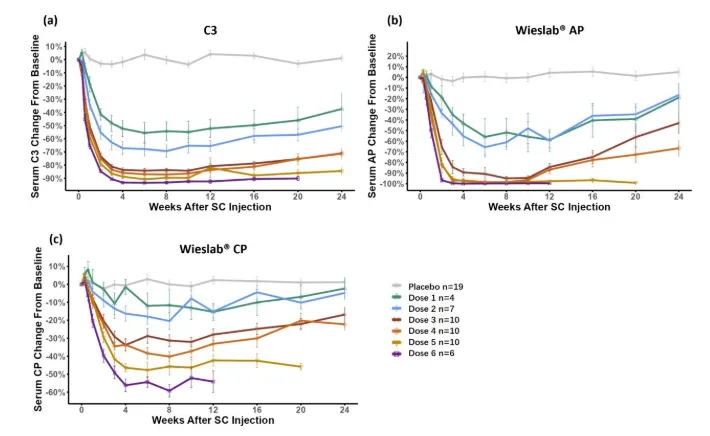
A Sylentis, uma empresa focada no desenvolvimento de medicamentos de RNAi, apresentou dois conjuntos de dados de estudos clínicos de Fase I para sua terapia de RNAi SGB{5}}9768, que tem como alvo o complemento C3, em formato de pôster. O SGB-9768 é o primeiro medicamento de siRNA na China direcionado ao complemento C3, utilizando a tecnologia proprietária da empresa GalNAc de entrega direcionada ao fígado para inibir especificamente a expressão de C3 via RNAi, suprimindo assim a ativação excessiva do sistema de complemento em sua fonte.
Os resultados dos ensaios clínicos de Fase I mostraram que uma única injeção subcutânea de SGB-9768 exibiu boa segurança e tolerabilidade, juntamente com reduções-dependentes da dose, significativas e sustentadas nos níveis de proteína C3 e inibição da atividade da via do complemento. Em comparação com outros produtos de siRNA direcionados à mesma via, o SGB-9768 alcançou níveis mais altos de redução da proteína alvo na mesma dose e manteve maior duração da eficácia do medicamento, demonstrando potencial como um "melhor-candidato da categoria". Com suas notáveis propriedades de ação prolongada, o SGB-9768 pode permitir intervalos de dosagem a cada três ou seis meses, melhorando bastante a conveniência do paciente. O medicamento entrou agora em ensaios clínicos de Fase II na China e recebeu a designação de medicamento órfão pelo FDA dos EUA para o tratamento da glomerulopatia C3.
02 Anticorpos/Proteínas de Fusão
Telitacicept: uma proteína de fusão de alvo duplo BLyS/APRIL-
Telitacicept, uma proteína de fusão de alvo duplo BLyS/APRIL-desenvolvida pela RemeGen, teve seus dados de ensaios clínicos de Fase III para o tratamento da nefropatia por IgA (IgAN) na China apresentados na ASN Kidney Week deste ano como uma "apresentação oral tardia-de ruptura".
Anteriormente, em agosto de 2025, a RemeGen anunciou que a-fase A deste estudo havia atingido seu objetivo primário: em comparação com o grupo placebo, os pacientes tratados com telitacicept alcançaram uma redução de 55% na proporção de proteína-para creatinina na urina de 24{{4}horas (UPCR) durante um período de tratamento de 39 semanas (P < 0,0001), com um perfil de segurança e tolerabilidade favorável. Dados detalhados deste estudo foram divulgados na reunião da ASN.
Com base nestes resultados positivos, o pedido de comercialização do telitacicept no tratamento da IgAN primária foi aceite pelo Centro de Avaliação de Medicamentos (CDE) na China e recebeu o estatuto de revisão prioritária, abrindo caminho para um acesso mais precoce para os pacientes chineses.
ODiretrizes de prática clínica chinesa para nefropatia por IgA em adultos e nefrite por vasculite por IgA (2025), lançado em outubro de 2025, incluiu o telitacicept pela primeira vez como uma proteína de fusão-de alvo duplo BLyS/APRIL. Ao inibir efetivamente a ativação de células-B e a produção de IgA, o medicamento demonstrou eficácia promissora em ensaios de Fase II e em vários estudos-do mundo real. A diretriz recomenda considerar o telitacicept como uma nova opção de tratamento para pacientes chineses com IgAN que permanecem em alto risco de progressão ou apresentam doença refratária, apesar da terapia de suporte adequada e do tratamento imunossupressor convencional.
Zigakibart: um anticorpo monoclonal direcionado a APRIL
Zigakibart é um novo anticorpo monoclonal humanizado que funciona ligando-se e bloqueando um ligante indutor de proliferação (APRIL). Ao fazer isso, reduz os níveis de IgA1 deficiente em galactose patogênica (Gd-IgA1) e bloqueia a formação de complexos imunes patogênicos, intervindo assim na progressão da doença de IgAN.
Na reunião da ASN, foram apresentados os resultados da análise de subgrupo do estudo ADU-CL-19 de Fase I/II de Zigakibart. Esta análise incluiu 35 pacientes do conjunto de análise de biomarcadores que tinham dados disponíveis na semana 100, com o objetivo de avaliar alterações da função renal a longo prazo em diferentes subgrupos com base nos níveis basais de TFGe e UPCR.
Os resultados mostraram que os pacientes estratificados pela TFGe basal mantiveram níveis estáveis de TFGe durante todo o período de tratamento de 100 semanas com Zigakibart. Da mesma forma, os pacientes agrupados por UPCR basal também exibiram uma tendência consistente de estabilidade da TFGe ao longo do curso de tratamento de 100 semanas. Esses achados sugerem que a eficácia do Zigakibart é independente da gravidade da doença e que pode proteger efetivamente a função renal, independentemente dos níveis basais de TFGe e UPCR dos pacientes.

03 Drogas de Moléculas Pequenas
Medicamentos de moléculas pequenas, com métodos de administração bem{0}}estabelecidos e claro valor clínico, desempenham um papel fundamental no tratamento da nefropatia por IgA (IgAN).
Nefecon: a primeira doença do mundo-modificando o tratamento para IgAN
As cápsulas de liberação-retardada de budesonida (nome comercial: Nefecon) são o primeiro agente terapêutico-modificador de doença do mundo para IgAN, funcionando como um imunomodulador que tem como alvo as células B na mucosa intestinal. Na reunião da ASN deste ano, foram apresentados sete novos estudos sobre Nefecon, explorando a sua eficácia e segurança no tratamento de IgAN em múltiplas dimensões.
As descobertas demonstraram que Nefecon oferece valor clínico significativo em três aspectos principais:terapia{0}modificadora da doença, intervenção precoce e tratamento-de longo prazo. Estudos-do mundo real confirmaram que Nefecon apresenta boa eficácia e segurança na prática clínica. A intervenção precoce desempenha um papel crucial na redução da proteinúria e na estabilização da função renal. Além disso, os dados de tratamento prolongado além de nove meses forneceram fortes evidências que apoiam sua eficácia e segurança a longo prazo.
Graças ao seu mecanismo inovador e às suas vantagens clínicas, Nefecon foi incluído tanto noDiretrizes de Prática Clínica KDIGO 2025 para o Tratamento da Nefropatia por IgA e Vasculite por IgAe oDiretrizes de prática clínica chinesa para nefropatia por IgA e vasculite por IgA em adultos (2025). Atualmente, é o único tratamento-modificador da doença para IgAN recomendado pelas diretrizes nacionais e internacionais, solidificando ainda mais seu papel fundamental na terapia de primeira-linha.
Iptacopan: Inibição de Precisão da Via Alternativa do Complemento
Desenvolvido pela Novartis, o iptacopan é o primeiro inibidor-da{1}}classe do fator de complemento B (CFB), direcionado aovia alternativa do complemento. Foi aprovado pela Administração Nacional de Produtos Médicos da China (NMPA) em setembro de 2025 para o tratamento de IgAN primária.
Na reunião da ASN, foram apresentados resultados provisórios do ensaio clínico APPLAUSE-IgAN Fase III em pacientes do Leste Asiático. O estudo incluiu 102 pacientes do Leste Asiático na análise de eficácia e 177 na análise de segurança. Os resultados mostraram que, em comparação com o placebo, o grupo iptacopan alcançou umRedução de 38,0% no UPCR de 24 horas em relação ao valor basal aos 9 meses, e umRedução de 36,5% na primeira-micção matinal (FMV) e na proporção de proteína-/{3}}creatinina na urina (UPCR-FMV).
Em termos de segurança, a incidência de eventos adversos{0}}relacionados ao tratamento foi semelhante entre os grupos iptacopan e placebo. O grupo iptacopan teve uma taxa de descontinuação do medicamento devido a eventos adversos de1.1%, comparado com2.2% no grupo placebo, indicando que o iptacopan é bem tolerado e tem um perfil de segurança favorável.

04 Conclusão
A nefropatia por IgA (IgAN), como a glomerulonefrite primária mais comum em todo o mundo, afeta uma grande população de pacientes e apresenta um alto risco de progressão da doença. De acordo com as estatísticas, prevê-se que o número global de pacientes com IgAN exceda10,2 milhões até 2030, com aproximadamente4,59 milhões de pacientes adultos na China-acabou100.000 novos casos anualmente, 80% deles são jovens e{1}}indivíduos de meia-idade com idade entre 20 e 59 anos. Mais alarmante,mais da metade dos pacientes diagnosticados podem progredir para doença renal-em estágio terminal (DRT) dentro de 20 anos, necessitando de-dependência vitalícia de diálise ou transplante renal. O custo da diálise só no primeiro ano pode atingir120.000 a 200.000 RMB, colocando um pesado fardo sobre as famílias e a sociedade.
De acordo com um relatório da Frost & Sullivan, otamanho do mercado global para terapêutica de nefropatia por IgAespera-se que cresça a partir567 milhões em 2020 para 1,196 bilhão em 2025, representando umtaxa composta de crescimento anual (CAGR) de 16,1%. Na China, prevê-se que o tamanho do mercado aumente de37 milhões em 2020 para 109 milhões em 2025, e espera-se que se expanda ainda mais paraUS$ 507 milhões até 2030.
Os numerosos resultados da investigação apresentados na ASN Kidney Week deste ano não só alcançaram avanços em termos de eficácia, como também continuaram a optimizar o tratamento em termos defrequência de dosagem, segurança e adequação para diversas populações de pacientes, oferecendo aos pacientes opções terapêuticas de{0}}maior qualidade. À medida que estes medicamentos inovadores avançam através dos ensaios clínicos e se tornam comercialmente disponíveis, eles têm o potencial dealiviar os encargos médicos e financeiros sobre os pacientes e a sociedade, trazendonova esperança para pacientes com nefropatia por IgA em todo o mundo.
Referências:
1.Sites oficiais das respectivas empresas
2.Site oficial da ASN
3.Títulos de código aberto






